ИНСТРУКЦИЯ по применению лекарственного препарата для медицинского применения
ИНФАНРИКС® ГЕКСА / INFANRIX® НЕХА (Вакцина для профилактики дифтерии, столбняка, коклюша (бесклеточная), полиомиелита (инактивированная), гепатита В комбинированная, адсорбированная в комплекте с вакциной для профилактики инфекции, вызываемой Haemophilus influenzae тип b конъюгированной, адсорбированной)
РЕГИСТРАЦИОННЫЙ НОМЕР: ЛП-000877
ТОРГОВОЕ НАИМЕНОВАНИЕ ПРЕПАРАТА: Инфанрикс® Гекса / Infanrix® Неxа
ГРУППИРОВОЧНОЕ НАИМЕНОВАНИЕ: вакцина для профилактики дифтерии, столбняка, коклюша (бесклеточная), гепатита В, полиомиелита (инактивированная), и инфекции, вызываемой Haemophilus influenzae тип b
ЛЕКАРСТВЕННАЯ ФОРМА: суспензия для внутримышечного введения в комплекте с лиофилизатом для приготовления суспензии для внутримышечного введения
СОСТАВ
| Наименование компонентов |
Количество в одной дозе 0,5 мл |
|
Вакцина для профилактики дифтерии, столбняка, коклюша (бесклеточная), полиомиелита (инактивированная), гепатита В комбинированная, адсорбированная |
|
|
Активные вещества |
|
| Анатоксин дифтерийный | не менее 30 МЕ |
| Анатоксин столбнячный | не менее 40 МЕ |
| Анатоксин коклюшный (АК) | 25 мкг |
| Гемагглютинин филаментозный (ФГА) | 25 мкг |
| Пертактин (Белок наружной мембраны 69 кДа) | 8 мкг |
| Антиген поверхностный рекомбинантный вируса гепатита B (HBsAg) | 10 мкг |
| Вирус полиомиелита 1 типа инактивированный | 40 ед. D-антигена |
| Вирус полиомиелита 2 типа инактивированный | 8 ед. D-антигена |
| Вирус полиомиелита 3 типа инактивированный | 32 ед. D-антигена |
|
Вспомогательные вещества |
|
| Натрия хлорид | 4,5 мг |
| Среда 199 (Медиум 199) (3) | 1,15 мг (включая аминокислоты 0,09 мг) |
| Алюминия гидроксид (4) | 0,5 мг |
| Алюминия фосфат (4) | 0,2 мг |
| Вода для инъекций | до 0,5 мл |
|
Вакцина для профилактики инфекции, вызываемой Haemophilus influenzae тип b конъюгированная, адсорбированная |
|
|
Действующее вещество |
|
| Капсульный полисахарид Haemophilus influenzae тип b, конъюгированный со столбнячным анатоксином 25 мкг | 10 мг |
|
Вспомогательные вещества |
|
| Лактоза | 12,6 мг |
| Алюминия фосфат | 0,12 мг |
(1) Содержание дифтерийного анатоксина 25 Lf (флоккулирующих единиц)
(2) Содержание столбнячного анатоксина 10 Lf (флоккулирующих единиц)
(3) Состав среды 199 (М199): кальция хлорида дигидрат — 185,50 мг/мл, железа нитрата нонагидрат — 0,10 мг/мл. калия хлорид — 400,00 мг/мл, калия дигидрофосфат -60,00 мг/мл, магния сульфата гептагидрат — 200,00 мг/мл, натрия хлорид — 8000,00 мг/мл. натрия гидрокарбонат — 350,00 мг/мл, натрия гидрофосфат — 47,50 мг/мл, L-аланин — 25,00 мг/мл, l-аргинина гидрохлорид — 70,00 мг/мл, l-аспарагиновая кислота — 30,00 мг/мл, 1-цистеина гидрохлорид — 0,099 мг/мл, L-цистин — 23,66 мг/мл, 1-глутаминовая кислота — 66,82 мг/мл, L-глутзмин -100,00 мг/мл, глицин -50,00 мг/мл, 1-гистидина гидрохлорида моногидрат — 21,88 мг/мл. 1-гидроксипролин -10,00 мг/мл, 1-изолейцин — 20,00 мг/мл, L-лейцин — 60.00 мг/мл, l-лизина гидрохлорид — 70.00 мг/мл. L-метионин -15.00 мг/мл, L-фенилаланин — 25,00 мг/мл, I пролин — 40.00 мг/мл, L-серин 25.00 мг/мл. 1-треонин — 30.00 мг/мл, L-триптофан -10,00 мг/мл. 1-тирозин — 40,00 мг/мл. L-валин — 25.00 мг/мл, аскорбиновая кислота 0.05 мг/мл, альфа-токоферол — 0,01 мг/мл, биотин — 0,01 мг/мл, кальциферол — 0,10 мг/мл. кальция пантотенат — 0,01 мг/мл, холина хлорид — 0,05 мг/мл, фолиевая кислота — 0,01 мг/мл, инозитол — 0.05 мг/мл, менадион — 0,019 мг/мл. никотиновая кислота — 0,025 мг/мл, никотинамид — 0,025 мг/мл, парз-аминобензойная кислота — 0.05 мг/мл, пиридоксаль гидрохлорид — 0,025 мг/мл, пиридоксина гидрохлорид — 0,025 мг/мл, рибофлавин — 0,01 мг/мл, тиамина гидрохлорид — 0,01 мг/мл, ретинола ацетат — 0,115 мг/мл, аденин -10,00 мг/мл. аденозина фосфат — 0.20 мг/мл. аденозина трифосфат натрия -10,00 мг/мл, холестерол — 0,20 мг/мл. дезоксирибоза 0,50 мг/мл, глюкоза -1000,00 мг/мл. глутатион — 0,05 мг/мл, гуанина гидрохлорид — 0,30 мг/мл. гипоксантин — 0,30 мг/мл, рибоза -0,50 мг/мл, натрия ацетат — 36,71 мг/мл, тимин — 0,30 мг/мл, Твин-80 — 5,00 мг/мл, урацил — 0,30 мг/мл, ксантин — 0,30 мг/мл.
(4) В пересчете на алюминий.
Инфанрикс® Гекса отвечает требованиям Всемирной Организации Здравоохранения (ВОЗ), относящимся к производству биологических субстанций и вакцин против дифтерии, столбняка и коклюша, а также вакцин против гепатита В, полученных методом рекомбинантной ДНК. инактивированных полиомиелитных вакцин, а также коньюгированных вакцин для профилактики инфекции, вызываемой Haemophilus influenzae тип b.
Вакцина не содержит консервантов.
ОПИСАНИЕ:
Вакцина для профилактики дифтерии, столбняка, коклюша (бесклеточная), полиомиелита (инактивированная), гепатита В комбинированная, адсорбированная: суспензия беловатого цвета, разделяющаяся при отстаивании на бесцветную прозрачную жидкость и белый осадок, полностью разбивающийся при встряхивании.
Вакцина для профилактики инфекции, вызываемой Haemophilus influenzae тип b, коньюгированная, адсорбированная: лиофилизированный порошок или плотная масса белого или серовато-белого цвета.
Восстановленный раствор, непрозрачная жидкость, при отстаивании разделяющаяся на бесцветную жидкость с образованием белого осадка, который легко ресуспендируется встряхиванием.
ФАРМАКОТЕРАПЕВТИЧЕСКАЯ ГРУППА: МИБП-вакцина.
Код ATX J07CA09.
ИММУНОЛОГИЧЕСКИЕ СВОЙСТВА
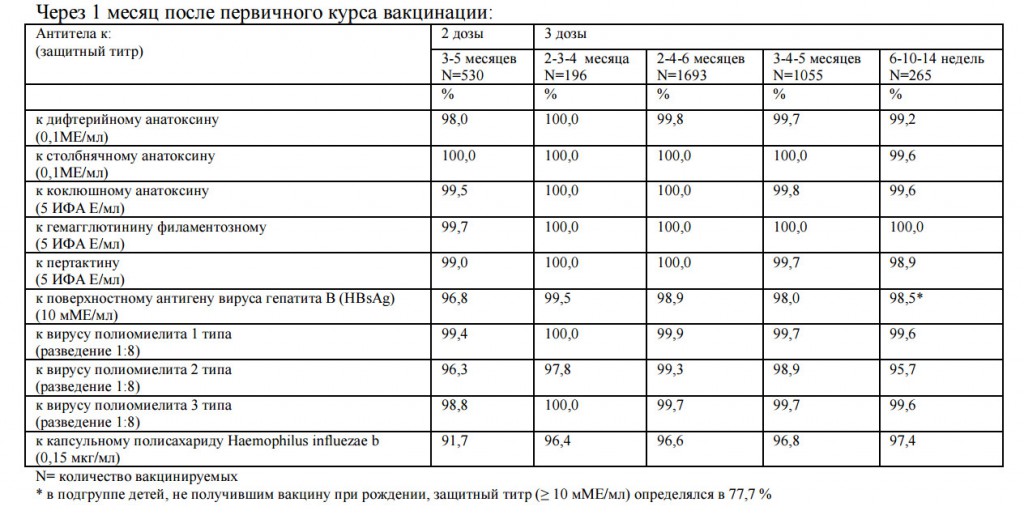
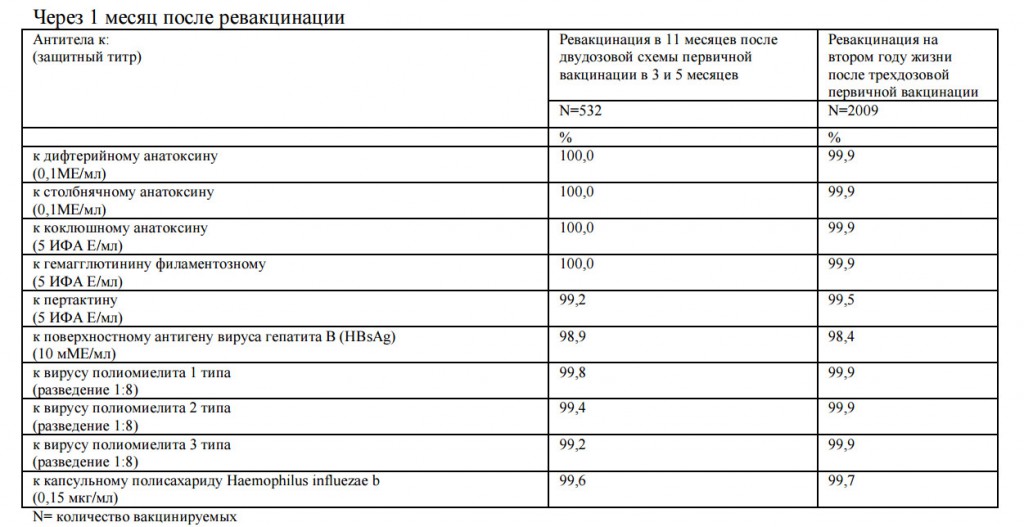
Иммуногенность
Антигенная активность компонентов вакцины Инфанрикс® Гекса не отличается от антигенной активности соответствующих моновакцин. При проведении первичной вакцинации на первом году жизни и ревакцинации на втором году жизни защитные титры составили:
Поскольку иммунный ответ на антигены коклюша в вакцине Инфанрикс® Гекса эквивалентен таковому на антигены коклюша в вакцине Инфанрикс®, ожидается, что защитная эффективность двух вакцин будет схожей.
Защитная эффективность в отношении коклюша
Защитная эффективность вакцины Инфанрикс® в отношении коклюша составляет от 84% до 88,7%, что подтверждено результатом клинических исследований, проведенных в Италии (2-4-6 месяцев) и Германии (3-4-5 месяцев). В Италии после завершения схемы первичной вакцинации против коклюша без проведения ревакцинации, защитная эффективность сохранялась в течение 60 месяцев у одной и той же группы лиц.
Длительность иммунного ответа
Защитная эффективность в отношении гепатита В сохранялась, по крайней мере, 3,5 года у более 90% детей, которым вводилось четыре дозы вакцины Инфанрикс® Гекса. Уровень антител не отличался от такового по сравнению с моновалентными вакцинами против гепатита В.
Данные пострегистрационного наблюдения
Эффективность Инфанрикс® Гекса в отношении инфекции, вызываемой Haemophilus influenzae тип b, была оценена в пострегистрационном исследовании в Германии и составила 89,6 % для лиц, получивших первичный курс вакцинации и 100 % для лиц, получивших первичный курс вакцинации и ревакцинацию.
Вакцина Инфанрикс® Гекса используется в Италии с 2006 года для профилактики коклюша у детей в возрасте 3, 5, 11 месяцев жизни, охват вакцинацией составляет свыше 95%. Сохраняется удовлетворительный контроль над гемофильной инфекцией: за период с 2006 по 2011 год в Италии ежегодно выявлялось не более 3% подтвержденных случаев гемофильной инфекции среди детей до 5 лет.
ПОКАЗАНИЯ ДЛЯ ПРИМЕНЕНИЯ
Первичная вакцинация и ревакцинация детей против дифтерии, столбняка, коклюша, гепатита В. полиомиелита и инфекции, вызываемой Haemophilus influenzae тип b.
ПРОТИВОПОКАЗАНИЯ ДЛЯ ПРИМЕНЕНИЯ
- Повышенная чувствительность к действующим веществам вакцины или к любому из компонентов вакцины, а также к неомицину и полимиксину.
- Повышенная чувствительность после предыдущего введения дифтерийной, столбнячной, коклюшной вакцин, вакцин против гепатита В, полиомиелита или инфекции, вызываемой Haemophilus influenzae тип b.
- Энцефалопатия неясной этиологии, развившаяся в течение 7 дней после предшествующего введения вакцины, содержащей коклюшный компонент. В этом случае введение вакцины против коклюша следует отменить, и продолжать вакцинацию только дифтерийно-столбнячной вакциной, а также вакцинами против гепатита В, полиомиелита и инфекции, вызываемой Haemophilus influenzae тип b.
- Острые инфекционные и неинфекционные заболевания, обострение хронических заболеваний являются временными противопоказаниями для проведения прививок Плановые прививки проводятся через 2-4 недели после выздоровления или в период реконвалесценции или ремиссии. При нетяжелых ОРВИ, острых кишечных заболеваниях и др прививки проводятся сразу после нормализации температуры.
ПРИМЕНЕНИЕ ПРИ БЕРЕМЕННОСТИ И ЛАКТАЦИИ
Поскольку вакцина Инфанрикс® Гекса применяется в соответствии с Национальным календарем профилактических прививок Российской Федерации у детей, нет данных о влиянии препарата на течение беременности и кормление грудью
СПОСОБ ПРИМЕНЕНИЯ И ДОЗЫ
Схемы вакцинации
Разовая доза вакцины составляет 0,5 мл.
Первичная вакцинация
Согласно Национальному календарю профилактических прививок Российской Федерации курс первичной вакцинации состоит из трех доз вакцины, вводимых в 3, 4,5 и 6 месяцев. Тем не менее, по рекомендации врача могут также применяться другие схемы трехдозовой (например 2-3-4 месяца, 3-4-5 месяцев, 2-4-6 месяцев) и двудозовой (например 3-5 месяцев) первичной вакцинации. Необходимо соблюдать интервал между дозами не менее 1 месяца.
Ревакцинация
Согласно Национальному календарю профилактически» прививок Российской Федерации ревакцинация проводится однократно в 18 месяцев жизни Тем не менее, по рекомендации врача ревакцинация может бытъ проведена в другое время при соблюдении интервала не менее 6 месяцев после последней прививки первичного курса Так, после двудозовой первичной вакцинации (например 3-5 месяцев) ревакцнирующую дозу предпочтительно вводить между 11 и 13 месяцем жизни, после трехдозового курса первичной иммунизации ревакцинирующая доза может быть введена до 18 мес. Во всеx случаях нарушения графика вакцинации врач должен руководствоваться инструкцией по применению лекарственного препарата и рекомендациями Национального календаря профилактических прививок Российской Федерации.
Способ введения
Рекомендуемое место введения—средняя треть переднелатеральной поверхности бедра. Вакцину следует вводить глубоко внутримышечно, чередуя стороны при последующих инъекциях.
Шприц, содержащий вакцину для профилактики дифтерии, столбняка, коклюша (бесклеточную), полиомиелита (инактивированную), гепатита В комбинированную, адсорбированную следует встряхнуть для получения однородной гомогенной суспензии беловатого цвета. Вакцину для профилактики дифтерии, столбняка, коклюша, гепатита В, полиомиелита комбинированную, адсорбированную и вакцину для профилактики инфекции, вызываемой Haemophilus influenzae тип b. конъюгированную, адсобированную необходимо визуально проверить на отсутствие механических включений и/или изменение внешнего вида. В случае их обнаружения следует отказаться от применения вакцины.
Для варианта упаковки с двумя иглами перед восстановлением вакцины с носика шприца необходимо снять защитный резиновый колпачок и плотно закрепить на шприце стерильную иглу, находящуюся в отдельном пластиковом контейнере. Для восстановления вакцины необходимо удалить с флакона, содержащего лиофилизат, защитную пластиковую крышечку и алюминиевый колпачок. Затем ввести суспензию, содержащуюся в шприце (вакцина для профилактики дифтерии, столбняка, коклюша (бесклеточная), полиомиелита (инактивированная), гепатита В комбинированная, адесобированная) через иглу во флакон с лиофилизатом (вакцина для профилактики инфекции, вызываемой Haemophilus influenzae тип b, конъюгированная, адсорбированная) путем прокалывания иглой резиновой пробки флакона. Содержимое ввести полностью.
Не отсоединяя шприц от флакона, необходимо дождаться полного растворения лиофилизата (не более 5 минут).
Восстановленная вакцина представляет собой более мутную суспензию по сравнению с исходной вакциной, использовавшейся для восстановления. В случае других изменений вакцина подлежит уничтожению. После восстановления вакцину необходимо полностью набрать обратно в шприц, сменить иглу и незамедлительно ввести. При этом восстановленная вакцина может находиться при комнатной температуре (21 °С) в течение 8 часов.
Предпочтительно введение вакцины после того, как она согреется до комнатной температуры. Кроме того, при комнатной температуре обеспечивается необходимая эластичность резиновой пробки флакона. Для этого флакон перед введением суспензии из шприца необходимо оставить при комнатной температуре (25 ± 3 °С) на пять минут.
Вакцина Инфанрикс® Гекса не применяется у детей старше 36 месяцев
ПОБОЧНОЕ ДЕЙСТВИЕ
Данные, полученные при проведении клинических исследований
Представленный ниже профиль безопасности основан на данных, полученных более чем у 16000 участников клинических исследовании.
При применении АКаДС и комбинированных вакцин, содержащих АКаДС–компоненты, наблюдалось увеличении частоты местных реакций и лихорадки после назначении ревакцинирующей дозы Инфанрикс® Гекса в 18 месяцев жизни, по сравнению с курсом первичной иммунизации.
Нежелательные явления, представленные ниже, перечислены по системам организма и в соответствии с частотой встречаемости. Частота встречаемости определяется следующим образом: очень часто (≥1/10), часто (≥1/100 и <1/10), нечасто (≥1/1000 и <1/100), редко (≥1/10000 и <1/1000), очень редко (<1/10000, включая отдельные случаи).
Частота встречаемости нежелательных явлений
Инфекционные и паразитарные заболевания
Нечасто: инфекции верхних дыхательных путей
Нарушения со стороны обмена веществ и питания
Очень часто: потеря аппетита
Нарушения психики:
Очень часто: раздражительность, необычный плач, беспокойство, возбудимость
Нарушения со стороны нервной системы:
Нечасто: сонливость
Очень редко: судороги (с лихорадкой или без нее)
Со стороны дыхательной системы, органов грудной клетки и средостения:
Нечасто: кашель (1)
Редко: бронхит
Нарушения со стороны желудочно-кишечного тракта:
Часто: рвота, диарея
Нарушения со стороны кожи и подкожных тканей:
Часто: зуд (1)
Редко: сыпь
Очень редко: дерматит, крапивница (1).
Общие расстройства и нарушения в месте введения:
Очень часто: болезненность, покраснение, отек в месте инъекции (≤50 мм2), повышение температуры тела ≥ 38 °С, утомляемость.
Часто: отек в месте инъекции (>50 мм2), повышение температуры тела > 39 °С, уплотнение в месте инъекции.
Нечасто: диффузный отек конечности, в которую была произведена инъекция, иногда с вовлечением прилежащего сустава (2).
Данные пострегистрационного наблюдения
При наблюдении за рутинным применением вакцины поступали сообщения о явлениях и симптомах (причинно-следственная связь многих перечисленных явлений с проведенной прививкой не установлена):
Нарушения со стороны крови и лимфатической системы:
лимфоаденопатия, тромбоцитопения.
Нарушения со стороны иммунной системы:
аллергические реакции (включаяанафилактические и анафилактоидные реакции, ангионевротический отек (1)).
Нарушения со стороны нервной системы:
коллапс или шокоподобное состояние (гипотензивно-гипореспонсивный синдром (3)).
Нарушения со стороны дыхательной системы, органов грудной клетки и средостения:
апноэ (1) ( см. Раздел«Особые указания»).
Общие расстройства и нарушения в месте введения:
выраженный отек, отек всей конечности, в которую была произведена инъекция (2), пузырьки в месте введения вакцины.
1 — наблюдается также при назначении других АКДС-вакцин и АКаДС-вакцин.
2 — у детей, получивших в качестве курса первичной вакцинации бесклеточные коклюшные вакцины, чаще развиваются местные реакции в виде припухлости после введения ревакцинирующей дозы, чем у детей, которым первичная вакцинация проводилась с использованием цельноклеточных вакцин. Такие реакции обычно проходят, в среднем, через 4 дня.
3 — анализ данных пострегистрационного наблюдения позволяет сделать вывод о потенциально повышенном риске развития судорог (на фоне повышенной температуры или без повышенной температуры тела) и гипотензивно-гипореспонсивного синдрома при совместном применении вакцины Инфанрикс® Гекса и вакцины Превенар 13 (вакцина пневмококковая полисахаридная конъюгированная адсорбированная, тринадцативалентная) по сравнению с применением только вакцины Инфанрикс® Гекса.
Опыт, полученный в ходе использования вакцины против гепатита В:
Во время пострегистрационного наблюдения после назначения вакцины против гепатита В производства компании «ГлаксоСмитКляйн Байолоджикалз с а.» у детей младше 2 лет были зарегистрированы следующие побочные явления (причинно-следственная связь с вакцинацией не установлена): менингит, синдром, напоминающий сывороточную болезнь, паралич, энцефалит, энцефалопатия, нейропатия, синдром Гийена-Барре, неврит, снижение АД, васкулит, плоский лишай, многоформная эритема, артрит, мышечная слабость.
ПЕРЕДОЗИРОВКА
Случаи передозировки не описаны
ВЗАИМОДЕЙСТВИЕ С ДРУГИМИ ЛЕКАРСТВЕННЫМИ ПРЕПАРАТАМИ
Пока недостаточно данных об эффективности и безопасности одновременного применения вакцины Инфанрикс® Гекса и вакцины против кори, эпидемического паротита и краснухи, что не позволяет предлагать какие-либо рекомендации об их совместном применении. Данные о совместном применении Инфанрикс® Гекса с вакциной Превенар (адсорбированной конъюгированной пневмококковой вакциной) показали отсутствие клинически значимого изменения в выработке антител против каждого из антигенов, входящих в состав вакцин, при их назначении в виде трехдозовой схемы первичной вакцинации. Однако была зарегистрирована более высокая частота встречаемости лихорадки (> 39,5 ° С) у детей, одновременно получавших Инфанрикс® Гекса и Превенар, по сравнению с детьми, получавшими только вакцину Инфанрикс® Гекса. В этом случае терапия жаропонижающими средствами должна быть начата в соответствии с местными рекомендациями Как и в отношении других вакцин, можно ожидать, что у пациентов, получающих иммуносупрессивную терапию, адекватный иммунный ответ может не достигаться. Вакцину Инфанрикс® Гекса нельзя смешивать с другими вакцинами в одном шприце
ОСОБЫЕ УКАЗАНИЯ
Перед вакцинацией следует изучить анамнез ребенка, обращая внимание на предшествующее введение вакцин и связанное с этим возникновение побочных реакций, а также провести осмотр.
Как и при введении любых других вакцин, следует иметь наготове все необходимое для купирования возможной анафилактической реакции на Инфанрикс® Гекса. Вакцинированный должен находиться под медицинским наблюдением в течение 30 минут после иммунизации.
Возникновение следующих реакций после введения вакцины Инфанрикс Гекса не является противопоказанием для последующих вакцинаций, однако при этом необходимо учитывать соотношение пользы и риска:
- температура ≥ 40 °С, возникшая в течении 48 часов;
- коллапс или шокоподобное состояние (гипотензивно-гипореспонсивный синдром), развившиеся в течение 48 ч после введения вакцины;
- непрекращяющийся плач, длящийся в течение трех часов и более, возникший в течение 48 ч после введения вакцины;
- судороги на фоне повышенной температуры тела или без повышенной температуры телавозникшие в течение 3 суток после вакцинации.
Инфанрикс Гекса следует применять с осторожностью у пациентов с тромбоцитопенией или с нарушениями системы свертывания крови, поскольку у таких пациентов внутримышечная инъекция может стать причиной кровотечения.
Как при любой другой вакцинации, не у всех вакцинированных может выявляться защитная иммунная реакция.
Инфанрикс Гекса не предотвращает развития заболеваний, вызванных какими-либо другими возбудителями, за исключением Corynebactetium diphthenae, Clostridium lelani, Bordetello pertussis, вируса гепатита В. вируса полиомиелита 1,2,3 типов и Haemophilus influenzae тип b. Однако ожидается профилактический эффект в отношении гепатита D. который может быть предотвращен с помощью вакцинации, т к гепатит D (вызванный вирусом гепатита дельта) не встречается в отсутствие вируса гепатита В.
Существуют ограниченные данные, основанные на вакцинации 169 недоношенных детей, свидетельствующие о том, что Инфанрикс Гекса может назначаться недоношенным детям. Однако у них может отмечаться более низкий иммунный ответ.
ВИЧ-инфекция не является противопоказанием к вакцинации. Однако после вакцинации пациентов с иммунодефицитом ожидаемый иммунологический ответ также может не достигаться.
Поскольку антиген капсульного полисахарида Haemophilus influenzae тип b экскретируется с мочой, в течение 1 -2 недель после вакцинации при анализе мочи может регистрироваться положительный тест. В этот период необходимо проведение других тестов для подтверждения диагноза инфекции, вызываемой Hаemophilus influenzae тип b.
У детей с прогрессирующими неврологическими расстройствами, включая инфантильные спазмы, неконтролируемую эпилепсию или прогрессирующую энцефалопатию, вакцинацию против коклюша (как цельноклеточными, так и бесклеточными вакцинами) необходимо отложить до стабилизации состояния. Решение о назначении вакцины с коклюшным компонентом должно быть принято индивидуально после тщательной оценки пользы и рисков.
Необходимо учитывать потенциальный риск апноэ и необходимость мониторинга дыхательной функции в течение 72 ч при первичной вакцинации детей, родившихся преждевременно (c 28 недель гестации) и, особенно, детей с респираторным дистресс-синдромом. Ввиду необходимости вакцинации детей данной группы, первичную вакцинацию не следует откладывать или отказывать в ее проведении. Первичный курс вакцинации таким детям следует осуществлять в условиях стационара под наблюдением врача в течение 72 ч.
Зарегистрирована более высокая частота встречаемости повышения температуры тела (> 39,5 ° С) у детей, одновременно получавших Инфанрикс® Гекса и Превенар, по сравнению с детьми, получавшими только вакцину Инфанрикс® Гекса.
Наблюдалось увеличения частоты встречаемости судорог (на фоне повышенной температуры или без повышенной температуры тела) и гипотензивно-гипореспонсивного синдрома при совместном применении вакцины Инфанрикс® Гекса и вакцины Превенар 13 (вакцина пневмококковая полисахаридная конъюгированная адсорбированная, тринадцативалентная) по сравнению с применением только вакцины Инфанрикс® Гекса (см. раздел «Побочное действие»).
После вакцинации или иногда перед ней возможны обмороки или выраженная слабость как психологическая реакция на инъекцию Перед вакцинацией важно удостовериться, что пациент не получит повреждений в случае обморока. Наличие фебрильных судорог в анамнезе, а также судорог в семейном анамнезе или синдрома внезапной детской смерти не является противопоказанием, но требует особого внимания. Таких вакцинируемых следует наблюдать в течение 2-3 дней, так как в этот период может возникнуть нежелательное явление.
ФОРМА ВЫПУСКА
Суспензия для внутримышечного введения в комплекте с лиофилизатом для приготовления суспензии для внутримышечного введения, 1 доза (0,5 мл).
Вакцина для профилактики дифтерии столбняка, коклюша (бесклеточная), полиомиелита (инактивированная), гепатита В комбинированная, адсорбированная (суспензия для внутримышечного введения) упакована: по 0,5 мл (1 доза) суспензии в шприц нейтрального стекла типа I (Евр.Ф.). Носик шприца укупорен колпачком из резины.
Вакцина для профилактики инфекции вызываемой Haemophilus influenzae b, конъюгированная, адсорбированная (лиофилизат для приготовления суспензии для внутримышечного введения) упакована: по 1 дозе лиофилизата во флакон нейтрального стекла типа I (Евр.Ф.), укупоренный пробкой из резины и алюминиевым колпачком под обкатку, снабженным защитной отщелкивающейся пластиковой крышечкой.
Комплектность
Для аптек
по 1 шприцу с суспензией и по 2 иглы (или без игл) в отдельных пластиковых контейнерах в комплекте с 1 флаконом с лиофилизатом в блистере из поливинилхлорида и закрытом пленкой из полиэтилентерефталата. По 1 блистеру вместе с инструкцией по применению в картонной пачке.
Для лечебно-профилактических учреждений
По 10 шприцев с суспензией и по 20 игл (или без игл) в мягкой контурной ячейковой упаковке в комплекте с 10 флаконами с лиофилизатом и инструкцией по применению в картонной коробке, снабженной встроенным картонным разделителем с защитной перфорацией от несанкционированного вскрытия
СРОК ГОДНОСТИ
3 года.
Не использовать после истечения срока годности, указанного на упаковке.
Датой окончания срока годности является последний день месяца, указанного на упаковке.
УСЛОВИЯ ХРАНЕНИЯ
Хранить при температуре от 2 до 8 °С.
Не замораживать.
Хранить в недоступном для детей месте.
УСЛОВИЯ ТРАНСПОРТИРОВАНИЯ
Транспортировать при температуре от 2 до 8 °С.
Не замораживать.
УСЛОВИЯ ОТПУСКА
Упаковка, содержащая 1 шприц в комплекте с 1 флаконом, — по рецепту.
Упаковка, содержащая 10 шприцев в комплекте с 10 флаконами, предназначена для лечебно- профилактических учреждений.
ПРОИЗВОДИТЕЛЬ
Производитель готовой лекарственной формы
«ГлаксоСмитКляйн Байолоджикалз с а.», Бельгия
Фасовщик (первичная упаковка)
«ГлаксоСмитКляйн Байолоджикалз с а.», Бельгия
«ГлаксоСмитКляйн Байолоджикалз с а.» — отделение СмитКляйн Бичем Фарма ГмбХ и Ко, КГ», Германия
Упаковщик (вторая (потребительская) упаковка)
«ГлаксоСмитКляйн Байолоджикалз с а.», Бельгия
«ГлаксоСмитКляйн Байолоджикалз с а.» — отделение СмитКляйн Бичем Фарма ГмбХ и Ко, КГ», Германия
«ГлаксоСмитКляйн Байолоджикалз», Франция
ООО «СмитКляйн Бичем-Биомед», Россия
Выпускающий контроль качества
«ГлаксоСмитКляйн Байолоджикалз с а.»/ GlaxoSmithKlme Biologicals s.a. Рю де л’Энститю, 89,1330 Риксенсарт, Бельгия / Rue de I’lnslitut, 89.1330 Rixensart, Belgium
ООО «СмитКляйн Бичем-Биомед, 143422, Московкая обл., Красногорский район, с. Петрово-Дальнее, ОАО «Биомед» им. И.И. Мечникова
НАИМЕНОВАНИЕ И АДРЕС ЮРИДИЧЕСКОГО ЛИЦА. НА ИМЯ КОТОРОГО ВЫДАНО РЕГИСТРАЦИОННОЕ УДОСТОВЕРЕНИЕ
ЗАО «ГлаксоСмитКляйн Трейдинг» 119180, г Москва. Якиманская наб. д 2 За дополнительной информацией обращаться: ЗАО «ГлаксоСмитКляйн Трейдинг»: 121614, Москва, Ул. Крылатская, дом 17, корп.3, эт.5, Бизнес-Парк «Крылатские Холмы»